Ergebnisse von Studien
CROVALIMAB
Crovalimab ist ein neuartiger C5-Inhibitor, der nach einer Aufsättigungsphase alle vier Wochen subkutan (unter die Haut) gespritzt wird. Patienten können dies selbst zu Hause durchführen und sind dadurch unabhängiger von den regelmäßigen Infusionsterminen in der Klinik, die bei anderen C5-Inhibitoren in den Alltag mit eingeplant werden müssen.
In 2 Phase 3 Studien wurde die Wirksamkeit und Sicherheit des Wirkstoffs untersucht und diese stellten sich als vergleichbar zu Eculizumab dar.
Das Wirkprinzip von Crovalimab unterscheidet sich gegenüber Eculizumab und Ravulizumab durch eine andere Bindungsstelle am C5-Protein und seine besondere Fähigkeit des Abbaus und zum Recycling und so die Dauer der Wirksamkeit verlängert.
In der einen Studie wurden 204 Patienten untersucht, die bisher noch keine Komplementinhibition erhalten hatten. Die Teilnehmenden wurden in einem Verhältnis von 2:1 in zwei Gruppen aufgeteilt. In der Gruppe A wurden die Teilnehmenden mit Crovalimab und in der Gruppe B wurden sie mit Eculizumab behandelt. Bei 79,3 % der Gruppe A konnte die Hämolyse kontrolliert werden (in Gruppe B waren es 79,0 %) und bei 65,7 % der Gruppe A konnten Transfusionen vermieden werden (in Gruppe B waren es 68,1 %).
Die häufigsten Nebenwirkungen waren insgesamt infusionsbezogene Reaktionen wie Kopf- (13,3 %) und Bauchschmerzen (1,5 %) in Gruppe A und Kopfschmerzen (8,7 %) in Gruppe B.
In der zweiten Studie wurden 89 Patienten untersucht, die vorher bereits Eculizumab oder Ravulizumab erhalten hatten und damit stabil eingestellt waren (Gruppe A). Die Hälfte der Teilnehmenden wechselte dann auf Crovalimab (Gruppe B). Auch hier konnte die Hämolyse in beiden Gruppen vergleichbar gut kontrollert werden und Transfusionen vermieden werden (68,1 % in Gruppe A und 65,7 % in Gruppe B). In Gruppe A traten bei 77 % der Teilnehmenden Nebenwirkungen auf, in Gruppe B 67 %. Keine der Nebenwirkungen führte zu einem Abbruch der Studie und kein Patient verstarb, ebenfalls traten keine Meningokokkeninfektionen auf.
Die häufigsten Nebenwirkungen in waren eine Typ-III-Hypersensitivität (bei Wechsel von Eculizumab auf Crovalimab), Infektionen der oberen Atemwege, Fieber, Kopfschmerzen und infusionsbedingte Reaktionen.
Die Daten zu Crovalimab im Vergleich zu Ravulizumab wurden bisher noch nicht veröffentlicht.
Crovalimab wurde im August 2024 in der EU und in Deutschland unter dem Handelsnamen Piasky® für PNH-Patienten ab 12 Jahren mit einem Gewicht von mind. 40 kg, die die Diagnose PNH haben und entweder Hämolyse mit Anzeichen für eine hohe Krankheitsaktivität haben (ohne PNH-spezifische Therapie) oder mindestens sechs Monate mit einem C5-Inhibitor behandelt wurden und dabei stabil sind, zugelassen.
Quellen:
Röth A, He G, Tong H, et al. Phase 3 randomized COMMODORE 2 trial: Crovalimab versus eculizumab in patients with paroxysmal nocturnal hemoglobinuria naive to complement inhibition. Am J Hematol. 2024; 99(9): 1768-1777. doi:10.1002/ajh.27412
Scheinberg P, Clé DV, Kim JS, et al. Phase 3 randomized COMMODORE 1 trial: Crovalimab versus eculizumab in complement inhibitor-experienced patients with paroxysmal nocturnal hemoglobinuria. Am J Hematol. 2024; 99(9): 1757-1767. doi:10.1002/ajh.27413
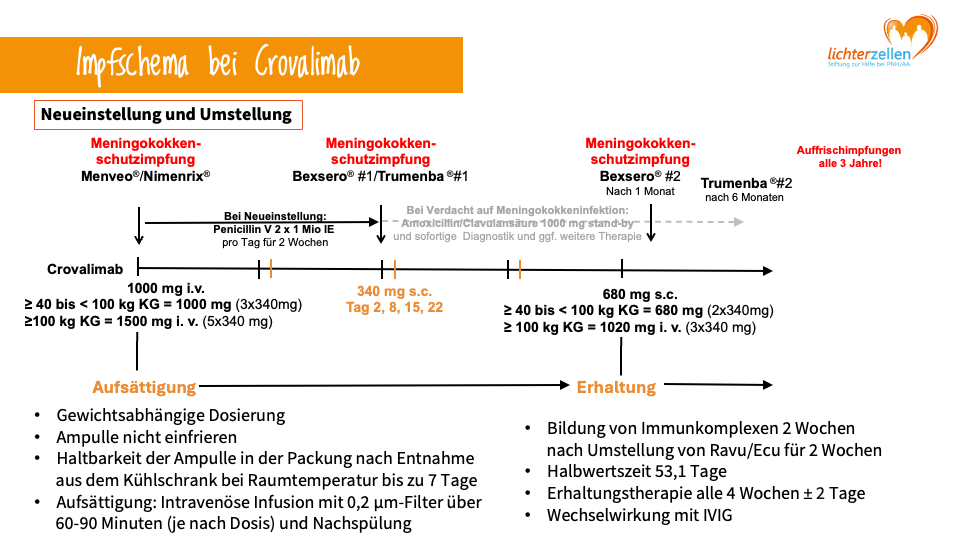
Quelle: Röth, A., Universitätsmedizin Essen